Dodecil Natriumsulfat (SDS) Struktur (SDS), Eigenschaften, verwendet
- 2855
- 500
- Ivan Pressler
Er Natriumsulfat -Dodecyl (SDS) ist ein anionischer, synthetischer und amphiphyllischer organischer Salz. Der apolare und hydrophobe Teil entspricht der Kohlenwasserstoffkette; Während der polar- und hydrophile Teil auf Sulfat mit negativer Belastung zurückzuführen ist.
Das SDS ist ein Tensid: seine Moleküle werden auf der Oberfläche wässriger Lösungen platziert, was zu einer Abnahme der Oberflächenspannung führt. Diese Funktion ermöglicht ihre Verwendung in Shampoo, Zahncremes, Seifen und anderen Artikeln zur persönlichen Pflege und der Reinigung von Eigenheimen.
 Natriumsulfat -Dodecilstruktur. Quelle: Benjah-BMM27 über Wikipedia.
Natriumsulfat -Dodecilstruktur. Quelle: Benjah-BMM27 über Wikipedia. Natriumsulfat -Dodecyl bindet an Protein und erzeugt seine Entfaltung, wobei eine längliche Form erfasst wird. Die Sulfatgruppen sind Wasser ausgesetzt und erwerben negative Lastproteine, deren Anzahl proportional zum Molekulargewicht ist.
Aus diesem Grund ermöglicht die SDS die Bestimmung der Molekulargewichte der Proteine durch Elektrophorese bei Polyacrylamid.
Obwohl eine mögliche krebserzeugende Wirkung der SDS vermutet wurde, wurde nicht eindeutig nachgewiesen, dass dies der Fall ist. SDs können wie andere Reinigungsmittel, Haut und Augenreizungen produzieren.
[TOC]
SDS -Struktur
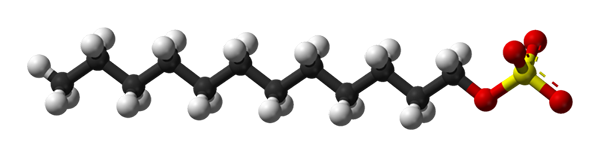
Im ersten Bild wurde das SDS -Molekül mit einem Kugeln und Balkenmodell gezeigt. Wie zu sehen ist, hat es einen hydrophoben und apolaren Kohlenstoffschwanz (schwarze und weiße Kugeln); Und gleichzeitig ein polarer Kopf dank der Gruppe der Gruppe -so4- (gelbe und rote Kugeln).
Obwohl nicht gezeigt wird, sollte es eine lila Kugel geben, die das nationale Kation darstellt+, direkt neben der Gruppe -so4-, elektrostatisch interagieren.
Das heißt, es wird mit dem bloßen Auge verstanden, warum diese Verbindung amphiphyllisch ist; und auch eine anionische Spannung, da die Last der SDS negativ ist und zusätzlich zu der NA andere Kationen anziehen kann+.
Das Molekül gibt den falschen Eindruck, starr zu sein, eine unbewegliche lineare Struktur. Es ist jedoch alles Gegenteil. Die SDs könnten mit einem „Wurm“ verglichen werden, dessen Kohlenstoffschwanz mehrere Schwingungen und Rotationen seiner einfachen Verbindungen aufweist. Dies macht ihn in der Lage, unterschiedliche Konformationen oder Falten in der Mitte anzuwenden; Zum Beispiel in Wasser.
Kristalle
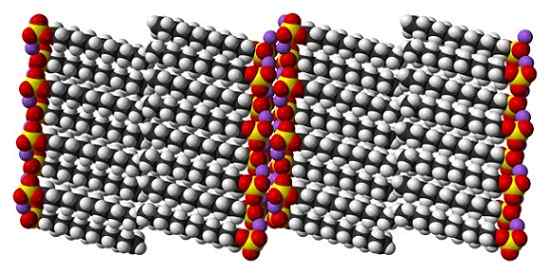 Kristallstruktur von Dodecyl -Natriumsulfat. Quelle: Benjah-BMM27 [Public Domain]
Kristallstruktur von Dodecyl -Natriumsulfat. Quelle: Benjah-BMM27 [Public Domain] Während es wahr ist, dass Natriumsulfat -Dodecyl ein dynamisches Molekül ist, muss es im Festzustand nicht zu viel bewegen und sich wie ein "einfacher" Balken verhalten. Und so werden jedes Molekül oder Stange so positioniert.
Kann Ihnen dienen: Natriumchlorit (NACLO2): Struktur, Eigenschaften, Verwendungen, RisikenDas Ergebnis ist die Bildung eines monoklinischen Kristalls, bei dem SDS -Moleküle in mehreren Stangensäulen (oberes Bild) verpackt werden (oberes Bild). Die intermolekularen Kräfte, die sie vereinen.
Mizellen
Außerhalb des Komforts seiner Kristalle kann das SDS -Molekül nicht mehr still bleiben; Fangen Sie an, seinen Schwanz zu verdrehen, um die Wechselwirkungen mit der äußeren Umgebung zu erhöhen oder zu verringern.
Wenn dieses Medium Wasser ist, tritt ein Phänomen, das als Micella -Bildung bezeichnet wird4-, Sie bleiben auf der Oberfläche, die mit H -Molekülen interagieren2ENTWEDER.
Dann erwirbt die Micella eine verlosene Ellipsoid -Morphologie (wie Erde, aber mehr zerquetscht). In dem Kristall sind sie wie Stangenblöcke und in einem wässrigen Medium wie Ellipsoidmizellen. Was wäre, wenn das Medium Öl wäre? Das Myce würde investiert werden: die polaren Köpfe so4- Sie würden in den Kern gehen, während ihre kohlensäurehaltigen Schwänze Öl ausgesetzt würden.
Eigenschaften
Namen
- Natriumdodecilsulfat (SDS).
- Natrium Laurilsulfat (SLS).
Molekularformel
C12H25ENTWEDER4Sna.
Molmasse
288,378 g/mol.
Physische Beschreibung
Mehrere Präsentationen: trockener Staub, flüssiger oder feuchter Feststoff. Seine Kristalle haben eine weiße oder cremige Färbung.
Geruch
Vater Geruch von fetten Substanzen, Toilette.
Schmelzpunkt
206 ºC.
Wasserlöslichkeit
1 · 105 mg/l. 1 g in 10 ml einer opaleszierenden Lösung gelöst.
Dichte
1,01 g/cm3.
Stabilität
Es ist unter den empfohlenen Speicherbedingungen stabil.
Zersetzung
Wenn er erhitzt wird, emittiert ein weißer Rauch aus Schwefeloxid und Natriumoxid.
Oberflächenspannung
39,5 Dynas/cm bei 25 ºC.
Kritische molare Konzentration
Ist 8,2 mm in reinem Wasser bei 25 ° C.
Anwendungen
Persönliche Pflege und Reinigung zu Hause
Sulfat -Dodecyl ist ein Tensid, das in zahlreichen Produkten wie Toilettenseifen, Schaumstoffbädern, Rasiermessercremes usw. verwendet wird. Es wird auch verwendet, um Flecken von Schwierigkeiten zum Löschen, bei der Reinigung der Böden und Badezimmern, der Furrying der Küchenartikel usw. zu entfernen.
Kann Ihnen dienen: Öl oder Benzinether: Formel, Struktur, verwendetTierärzte und Humanmedizin
Es wird als Abstoßung von Flöhen und Zecken verwendet, die bei Tieren vorhanden sind. Es wird auch als Feuchtigkeitscreme in einigen Antibiotika für den oralen oder topischen Gebrauch verwendet.
Das SDS ist Mikrobizid gegen Viren mit Verpackung wie HIV, Typen 1 und 2 und das Herpes-Herpes-Virus (HSV-2). Es wirkt auch auf Virus ohne Verpackung: Papillomavirus, Reovirus, Rotavirus und Poliovirus. Diese Verwendung ist jedoch nicht genehmigt.
Die Verwendung von SDs wurde als vaginale Dusche vorgeschlagen, die Schutz gegen sexuell übertragbares Virus ermöglicht. Auch in der Muttermilchverarbeitung, um die Möglichkeit einer HIV -Übertragung durch Stillen zu beseitigen oder zu verringern.
Zusätzlich zu seiner antiviralen Wirkung wirkt das SDS auf pathogene Bakterien und Pilze. SDS eliminiert Arzneimittelresistenz und sexuelle Resistenzfaktoren von e. coli; und blockiert das Wachstum zahlreicher positiver Grammbakterien.
Im Labor
Das SDS bindet an Proteine, die ihre Denaturierung verursachen, negative Belastungen und eine Konformationsänderung liefern. Dies ermöglicht die Bestimmung seiner Molekulargewichte durch Elektrophorese in Polyacrylamid.
SDS wird auch zur Herstellung von Hirngewebeproben zur Verwendung in der optischen Mikroskopie verwendet. Es wird auch zur Herstellung von Blutproben für die Anzahl der Erythrozyten verwendet.
Das SDS wird zur Reinigung von Nukleinsäuren verwendet, da sie die Membranen auflösen können.
Darüber hinaus wird der SDS zur Charakterisierung von quaternären Ammoniumverbindungen verwendet.
Lebensmittelzusatz
SDS wird als Emulgator- und Nahrungsmittelverdickung verwendet. Verbessert die Stabilität und Textur von gebackenen Produkten. Zusätzlich wird es als Hilfsmittel in getrockneten Eierprodukten verwendet.
Kann Ihnen dienen: Zinknitrat: Struktur, Eigenschaften, erhalten, verwendet, verwendetIndustrie
Das SDS wird in der Galvanoplastikindustrie verwendet, insbesondere in Nickel und Zink; als emulgierende und durchdringende Lack und Malerei; in der Formulierung von explosiven durch Injektion geformten; und in festen Raketen wie Schaum.
Risiken
SDS Konstante Exposition kann bei Meerschweinchen Hauthyperplasie verursachen. Kaninchen und Menschen sind weniger anfällig für diese Verletzungen. Direkter Kontakt mit SDs bei einer Konzentration von ≤ 20%kann eine mäßige Entzündung und Hautreizungen verursachen.
Andererseits kann eine längere Exposition gegenüber SDS Dermatitis mit Anzeichen von Rötung, Schwellung und Ampullenbildung erzeugen.
SDs können durch Kontakt Augenreiz erzeugen. Bei manchen Menschen kann es auch sehr reaktiv sein und die Reizung von Atemwege und Atemnot inhalieren lassen.
Selten kann die Einnahme von SDS ätzende Läsionen verursachen. Es wurde jedoch bei Kindern berichtet, die SDs aufgenommen haben, das Erbrechen der schnellen Entwicklung, die ZNS -Depression und die Atemnot aufgenommen haben.
In der SDS wurden keine Genotoxizität oder teratogene Wirkung festgestellt. Bei 242 Patienten mit ekzematöser Dermatitis wurden 6,4 % der Patienten mit Allergien gefunden, was auf die Verwendung von SDs zurückzuführen ist.
Verweise
- Strukturdaten aus l. ZU. Smith, r. B. Hammond, k. J. Roberts, d. Maschin, g. McLeod (2000). Bestimmung der Kristallstrecke von wasserfreiem Natriumdodecylsulfat unter Verwendung einer Kombination aus Sychrotron -Strahlungspulverbeugung und molekularen Modellierungstechniken. Journal of Molekularstruktur 554 (2-3): 173-182. Doi: 10.1016/s0022-2860 (00) 00666-9.
- Wikipedia. (2019). Natriumdodecylsulfat. Abgerufen von: in.Wikipedia.Org
- Nationales Zentrum für Biotechnologie Information. (2019). Natriumdodecylsulfat. Pubchem -Datenbank. CID = 3423265. Erholt von: Pubchem.NCBI.NLM.NIH.Regierung
- Hammouda b. (2013). Temperatureffekt auf die Nanostruktur von SDS -Mizellen im Wasser. Journal of Research des National Institute of Standards and Technology, 118, 151-167. Doi: 10.6028/jres.118.008
- Elsevier. (2019). Natriumdodecylsulfat. Wissenschaft direkt. Abgerufen von: Scientedirect.com
- Kumar, s., Thejajenuo, j. K. und Tsipila, t. (2014). Toxikologische Wirkungen von Natriumdodecylsulfat. Journal of Chemical and Pharmaceutical Research 6 (5): 1488 - 1492.
- Toxicology Data Network. (S.F.). Natriumlaurylsulfat. Toxnet. Wiederhergestellt von: Toxnet.NLM.NIH.Regierung

