Ethylenoxidstruktur, Eigenschaften, Risiken und Verwendung
- 4131
- 401
- Tizian Liebich
Er Ethylenoxid Es ist eine organische Verbindung der Epoxidefamilie. Bei Raumtemperatur ist es gasförmig, farblos und obwohl es sich fast um Toilette handelt, hat es einen weichen süßen Geruch, ähnlich wie bei den Ether.
Es handelt. Dies ist auf seine hohe Reaktivität zurückzuführen, dh auf seine Leichtigkeit, mit anderen Substanzen zu reagieren.
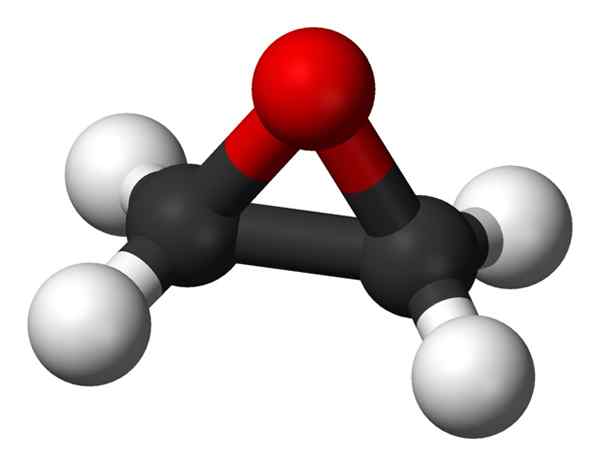
 Räumliche Struktur von Ethylenoxid. Schwarze Kugeln: Kohlenstoffatome; Weiße Kugeln: Wasserstoffatome; Roter Kugel: Sauerstoffatom. Benjah-BMM27 [Public Domain]. Quelle: Wikimedia Commons.
Räumliche Struktur von Ethylenoxid. Schwarze Kugeln: Kohlenstoffatome; Weiße Kugeln: Wasserstoffatome; Roter Kugel: Sauerstoffatom. Benjah-BMM27 [Public Domain]. Quelle: Wikimedia Commons. Eine seiner Hauptanwendungen ist ein Rohstoff bei der Herstellung der Komponenten von Frostschutzmittel für Fahrzeugheizkörper. Seine Derivate werden als Zutaten von Industrie- oder Heimreinigern, kosmetischen Produkten und Shampoos, plastifizierenden, pharmazeutischen Präparaten oder Salben eingesetzt.
Es ist ein weit verbreitetes Desinfektionsmittel, beispielsweise bei der Sterilisation von medizinischen und zahnärztlichen Geräten, da es in der Lage ist, Viren, Bakterien, Pilze und Sporen zu zerstören, insbesondere unter trockenen Bedingungen. Darüber hinaus wurde es verwendet, um Lebensmittelprodukte für Ihre Verpackung zu räumen, obwohl diese Verwendung in Frage gestellt wird.
Trotz seiner Nützlichkeit muss es mit hoher Vorsicht manipuliert werden, da es Reizungen der Augen und der Haut verursachen kann. Das Einatmen von Ethylenoxid über lange Zeiträume kann das Nervensystem beeinflussen. Daher müssen Personen, die ihren Dämpfen oder Lösungen ausgesetzt sind.
[TOC]
Struktur
Seine molekulare Formel ist c2H4ENTWEDER. Es gehört zur Gruppe der Epoxide und ist die einfachste und wichtigste davon. Es hat die Form eines Drei -Mitglieds -Rings.
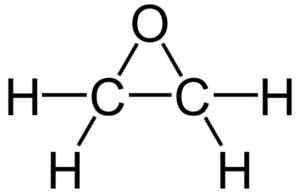 Ethylenoxidstruktur. Quelle: Wikimedia Commons
Ethylenoxidstruktur. Quelle: Wikimedia Commons Aufgrund seiner dreieckigen Ringstruktur ist Ethylenoxid sehr reaktiv, was auf die Leichtigkeit zurückzuführen ist, mit der sich der Ring öffnet. Im Durchschnitt sind die Verbindungswinkel 60º, wodurch ihre Glieder schwach werden. Das Molekül ist weniger stabil als das eines linearen Ethers und reagiert dazu, leicht mit anderen chemischen Verbindungen zu reagieren.
Kann Ihnen dienen: Natriumnitrit (Nano2): Struktur, Eigenschaften, Verwendungen, RisikenEigenschaften
Andere Namen
- Oxyran.
- Epoxietano.
Körperlicher Status
Bei Raumtemperatur und unter atmosphärischem Druck ist es ein Gas. Unter 10,6 ° C und unter atmosphärischem Druck ist es eine Flüssigkeit. Unter -111 ºC ist ein Feststoff.
Molekulargewicht
44,05 g/mol.
Flammpunkt
Weniger als 0 ºF (-17,8 ºC).
Dichte
Seine Dichte ist geringer als die von Wasser und beträgt 0,882 bis 10 ° C. Wiederum sind ihre Dämpfe schwerer als Luft.
Löslichkeit
Es ist löslich in Wasser, Benzol, Aceton, Ethanol und Ether. Es ist mit Kohlenstoff -Tetrachlorid mischbar.
Selbstdirektionstemperatur
428,9 ºC.
Andere Eigenschaften
- Wenn es einem Heizung oder Kontamination unterzogen wird, kann es exothermisch polymerisieren (erzeugt eine große Menge Wärme). Wenn eine Polymerisation in einem Behälter auftritt, kann sie gewaltsam gebrochen werden.
- Kann mit oxidierenden Materialien reagieren.
- Es ist extrem giftig, karzinogen und guter Mutationengenerator in Bakterien und Säugetierzellen.
Produktion
Im industriellen Maßstab wird es durch Oxidation von Ethylen mit Sauerstoff hergestellt (oder2) aus der Luft. Die Geschwindigkeit dieser Reaktion wird mit dem Vorhandensein von Silbermetall (AG) und Temperaturwirkung erhöht. Als nächstes wird die Reaktion gezeigt:
Ag, 250ºC
2 c2H4 + ENTWEDER2 -> 2c2H4ENTWEDER
Ethylenethylenoxid
Risiken
Für die Gesundheit
- Es wurde berichtet, dass es neurologische Störungen erzeugt und dass der Tod verursachen kann. Die niedrigere Konzentration, die durch Inhalation toxische Wirkungen erzeugen kann.500 ppm/10 Sekunden (ppm bedeutet: Teile pro Million).
- Es ist eine starke irritierende Haut, Augen und Atemwege.
Kann Ihnen dienen: Samario: Eigenschaften, Struktur, erhalten, verwendet, verwendet- Dampfexposition mit hoher Ethylenoxidkonzentration kann Augenreizungen, Entzündungen der Augenmembran und Hornhautschäden verursachen.
- Die Entwicklung von Katarakten wurde mit der Exposition gegenüber ihren Dämpfen und Spritzern in Verbindung gebracht. Bei konzentrierten Lösungen gibt es den Augen schwere Schäden.
- Der Kontakt von wässrigen Ethylenoxidlösungen mit der Haut erzeugt Reizungen und kann zu schwerer Dermatitis mit Ampullen und Verbrennungen führen.
- Die Inhalation kann das Nervensystem beeinflussen und Kopfschmerzen und Übelkeit verursachen, unter anderem Symptome.
Feuer
- Wenn es einer Flamme oder Wärme ausgesetzt ist, besteht eine Explosionsgefahr. Wenn sie erhitzt werden, erzeugen sie gefährliche Dämpfe.
- Dampf bildet explosive Gemische mit Luft in einem weiten Bereich von Konzentrationen.
- Es sollte vermieden werden, es mit Geräten zu manipulieren, die Metalle wie Kupfer, Silber, Quecksilber, Magnesium, Aluminium oder Eisenoxide sowie Gegenstände wie Ammoniak, Oxidationsmittel, Säuren oder organische Basen vermeiden. Alle diese Materialien können ihre Polymerisation und/oder Explosion beschleunigen.
Anwendungen
Industrielle Anwendungen
Es wird als Vermittler bei der Herstellung anderer Chemikalien verwendet, die wiederum bei der Herstellung von Polyesterfasern für Kleidung, Polsterung, Teppiche und Kissen verwendet werden.
Mit Ethylenoxid wird Ethylenglykol im Frostschutzmittel für Fahrzeugmotoren verwendet. Ethylenglykol wird auch in der Herstellung von Glasfaser- und Plastikfilmen zur Verpackung verwendet.
Andere aus Ethylenoxid hergestellte Chemikalien umfassen nichtionische Tenside, die in Reinigungsmitteln und Formeln verwendet werden, um die Gerichte zu waschen.
Kann Ihnen dienen: Isobutil: Nomenklatur, Schulung, Struktur und EigenschaftenMedizinische Anwendungen
Es wird als Sterilisationsmittel von medizinischen Geräten wie chirurgischen Instrumenten, Injektoren und Injektoren oder Prothesen verwendet.
Es wird auch verwendet, um Maschinen für Hämodialyse, Laborgeräte, Zahninstrumente, Tierärzte, Thermometer, chirurgische Kleidung oder Erste -Hilfe -Geräte zu sterilisieren.
 Sterilisationsraum. Quelle: Pixabay.com
Sterilisationsraum. Quelle: Pixabay.com Obwohl für die Sterilisation medizinischer Geräte verschiedene Methoden verfügbar sind, kann in einigen Verwendungszwecken keine verfügbare Behandlung Ethylenoxid ersetzen.
Dies ist der Fall bei der Sterilisation bestimmter Wärmeematerialien und Strahlung sowie einiger Instrumente und Artefakte, die Sterilisation am Ort der Krankenhäuser selbst erfordern.
Bibliotheken und Museen
An diesen Orten wird Ethylenoxid verwendet, um Schädlinge wie Pilze und Insekten zu kontrollieren. Diese Verwendung ist jedoch nicht so häufig und wird verwendet, wenn andere Alternativen nicht wirksam sind.
Landwirtschaft und Nahrung
Es wurde unter anderen Varianten als Pestizid, Fungizid, faszant, Herbizid, Insektizid und Rodentizid verwendet. Reduziert die Population von Bakterien- und Gewürzenpilzen erheblich.
Aufgrund von Sicherheits- und Umweltproblemen wurde jedoch in der Europäischen Union und in den USA Ethylenoxid für Lebensmittelausströmung verboten.
Verweise
- ODER.S. Nationalbibliothek für Medizin. (2019). Ethhylenoxid. Aus Pubchem geborgen.NCBI.NLM.NIH.Regierung
- Chemische Sicherheitsfakten. (2019). Ethhylenoxid. Von Chemicals -Sicherheitsfakten gewonnen.Org
- Morrison, Robert Thornton; und Boyd, Robert Neilson. 1992. Organische Chemie. Prentice-Hall.
- Moerman, f. und Mager, k. (2016). Reinigung und Entfernung in Trockennahrungsmittelverarbeitungseinrichtungen. In Handbook of Hygiene Control in der Lebensmittelindustrie (zweite Ausgabe). Von Scientirect erholt.com.
- Eastmond, David a. und Balakrishnan, Sharada. (2010). Genotoxie von Pestiziden. In Hayes 'Handbuch für Pestizidtoxikologie (dritte Ausgabe). Von Scientedirect erholt.com
- Atungulu, g.G. und Brot, z. (2012). Mikrobielle Dekontamination von Nüssen und Gewürzen. In der mikrobiellen Dekontamination in der Lebensmittelindustrie. Von Scientedirect erholt.com
- « Eisenoxid (ii) Struktur, Nomenklatur, Eigenschaften, verwendet
- Einfache flache Epitheleigenschaften, Funktionen und Typen »

