Boltzmann Konstante Geschichte, Gleichungen, Berechnung, Übungen

- 2094
- 414
- Said Ganzmann
Der Boltzmann Konstante Es ist der Wert, der die durchschnittliche kinetische Energie eines thermodynamischen Systems oder eines Objekts mit der absoluten Temperatur derselben bezieht. Obwohl sie oft verwirrt sind, sind Temperatur und Energie nicht das gleiche Konzept.
Die Temperatur ist ein Maß für die Energie, aber nicht die Energie selbst. Mit der Boltzmann -Konstante ist man wie folgt miteinander verbunden:
UNDC = (3/2) kB T
 Boltzmann Wirt in Wien. Quelle: Dadotet bei English Wikipedia [CC BY-SA 3.0 (http: // creativecommons.Org/lizenzen/by-sa/3.0/]]
Boltzmann Wirt in Wien. Quelle: Dadotet bei English Wikipedia [CC BY-SA 3.0 (http: // creativecommons.Org/lizenzen/by-sa/3.0/]] Diese Gleichung gilt für ein ideales monoatomisches Gasmolekül M, Wo UNDC Es ist seine kinetische Energie in Joule, kB Es ist Boltzmanns Konstante und T Es ist die absolute Temperatur in Kelvin.
Auf diese Weise steigt die durchschnittliche kinetische Energie durch Substanzmolekül, wie erwartet die durchschnittliche kinetische Energie steigt. Und das Gegenteil tritt auf, wenn die Temperatur abnimmt und in der Lage ist, den Punkt zu erreichen, an dem die gesamte Bewegung aufhört, die niedrigste oder absolute Temperatur erreicht wird.
Wenn Sie über durchschnittliche kinetische Energie sprechen, müssen sich erinnern, dass kinetische Energie mit Bewegung verbunden ist. Und die Partikel können sich in vielerlei Hinsicht bewegen, z. B. sich bewegen, drehen oder vibrieren. Natürlich wird es nicht alle auf die gleiche Weise tun, und da sie unzählig sind, wird der Durchschnitt genommen, um das System zu charakterisieren.
Einige Energiezustände sind wahrscheinlicher als andere. Dieses Konzept ist in der Thermodynamik von radikaler Bedeutung. Die in der vorherigen Gleichung betrachtete Energie ist die kinetische Übersetzungsergie. Von der Wahrscheinlichkeit der Staaten und ihrer Beziehung zur Boltzmann -Konstante wird etwas später sprechen.
2018 wurde das Kelvin neu definiert und mit ihm die Boltzmann -Konstante, die im internationalen System ungefähr 1 ist.380649 x 10-23 J. K-1. Für die Boltzmann -Konstante, die in zahlreichen Laboratorien auf der ganzen Welt mit verschiedenen Methoden bestimmt wurde, kann viel mehr Präzision erreicht werden.
[TOC]
Geschichte
Die berühmte Konstante verdankt dem Physiker Ludwig Boltzmann (1844-1906), der in Wien geboren wurde und sein Leben als Wissenschaftler der Untersuchung des statistischen Verhaltens der Systeme mit vielen Partikeln widmete, aus der Sicht der Newtonischen Mechanik.
Obwohl heute die Existenz des Atoms allgemein anerkannt wird, wurde im neunzehnten Jahrhundert der Glaube darüber, ob das Atom wirklich existierte oder mit dem viele physikalische Phänomene erklärt wurden.
Kann Ihnen dienen: Normaler Vektor: Berechnung und BeispielBoltzmann war ein starker Verteidiger der Existenz des Atom.
Er erklärte, dass beobachtbare Phänomene auf makroskopischen Ebenen durch die statistischen Eigenschaften von Bestandteilen wie Atomen und Molekülen erklärt werden könnten.
Diese Kritik kann auf die tiefe Episode der Depression zurückzuführen sein, die ihn Anfang September 1906 das Leben nahm, als er noch viel zu tun hatte, weil er als einer der großen theoretischen Physiker seiner Zeit und dort angesehen wurde Es war wenig zu diesen Wissenschaftlern, die zur Bestätigung der Richtigkeit ihrer Theorien beitragen werden.
Es geschah nicht lange nach seinem Tod, als neue Entdeckungen über die Natur des Atoms und seine Bestandteile hinzugefügt wurden, um Boltzmann den Grund zu geben.
Boltzmanns Konstante und Plancks Werke
Nun, Boltzmanns Konstante kB Es wurde eingeführt, wie es heute eine Weile nach der Arbeit des österreichischen Physikers bekannt ist. Es war Max Planck, in seinem Gesetz der Emission des schwarzen Körper23 J/k.
Bis zum Jahr 1933 wurde Boltzmann zu Wien als Plakat -Tribut eine Plakette mit der Definition der Entropie mit der berühmten Konstante hinzugefügt: S = kB Protokoll w, Gleichung, die später diskutiert wird.
Heute ist Boltzmanns Konstante bei der Anwendung der thermodynamischen Gesetze, der statistischen Mechanik und der Informationstheorie unverzichtbar, deren Bereiche dieser Physiker mit traurigen Ende ein Pionier war.
Wert und Gleichungen
Gase können makroskopisch und auch mikroskopisch beschrieben werden. Für die erste Beschreibung gibt es Konzepte wie Dichte, Temperatur und Druck.
Es sollte jedoch daran erinnert werden, dass ein Gas aus vielen Partikeln besteht, die eine globale Tendenz zu einem bestimmten Verhalten haben. Es ist dieser Trend, der makroskopisch gemessen wird. Eine Möglichkeit, die Konstante von Boltzmann zu bestimmen, ist die gut bekannte Gleichung idealer Gase:
P.V = n. R. T
Hier P Es ist Gasdruck, V Es ist sein Volumen, N Es ist die Anzahl der vorhandenen Maulwürfe, R Es ist die Konstante der Gase und T Es ist die Temperatur. In einem Mol idealer Gas ist die folgende Beziehung zwischen dem Produkt erfüllt P.V, und die kinetische Übersetzungsergie K Das ganze Set ist:
Kann Ihnen dienen: Korpuskuläres Modell der MaterieP.V = (2/3). K
Kinetische Energie ist daher:
K = (3/2) n.R.T
Durch die Teilen durch die Gesamtzahl der vorhandenen Moleküle, die als N bezeichnet werden, wird die durchschnittliche kinetische Energie eines einzelnen Partikels erhalten:
UNDC = K /n
UNDC= (3/2n) n.R.T
In einem Mol gibt es die Anzahl der Partikel nZU, Und daher ist die Gesamtzahl der Partikel N = nnA, bleiben:
UNDC = (3/2nnZU) N.R.T
Genau der Quotient R/nZU Es ist Boltzmanns Konstante und wird gezeigt, dass die kinetische Energie der durchschnittlichen Translation eines Partikels nur von der absoluten Temperatur und nicht von anderen Größen wie Druck, Volumen oder sogar der Art des Moleküls abhängt:
UNDC = (3/2) kB. T
Boltzmanns Konstante und Entropie
Ein Gas hat eine bestimmte Temperatur, aber diese Temperatur kann unterschiedlichen inneren Energiezuständen entsprechen. Wie man diesen Unterschied visualisieren?
Betrachten Sie den gleichzeitigen Start von 4 Münzen und die Art und Weise, wie sie fallen können:
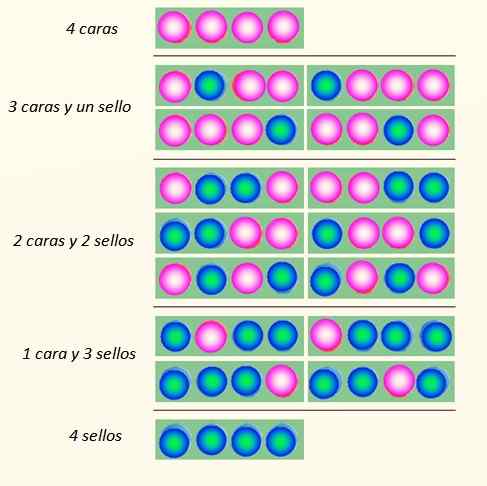 Wege, auf denen 4 Münzen fallen können. Quelle: Selbst gemacht
Wege, auf denen 4 Münzen fallen können. Quelle: Selbst gemacht Der Münzsatz kann insgesamt 5 Staaten annehmen, die berücksichtigt werden Makroskopisch, beschrieben in der Abbildung. Welcher dieser Staaten würde der Leser sagen, dass es das wahrscheinlichste ist??
Die Antwort sollte der Zustand von 2 Gesichtern und 2 Kreuzen sein, da sie insgesamt 6 Möglichkeiten hat, der 16 in der Figur dargestellt. Und 24 = 16. Diese entsprechen den Staaten mikroskopisch.
Und was ist, wenn 20 Münzen anstelle von 4 gestartet werden? Es würde insgesamt 2 gebenzwanzig Möglichkeiten oder "mikroskopische Zustände". Es ist eine viel größere und schwierigere Zahl zu behandeln. Um die Verwaltung großer Zahlen zu erleichtern, sind Logarithmen sehr angemessen.
Nun, was offensichtlich erscheint, ist, dass der Staat mit der größten Störung der wahrscheinlichste ist. Die am meisten bestellten Zustände wie 4 Gesichter oder 4 Briefmarken sind etwas weniger wahrscheinlich.
Die Entropie eines makroskopischen Zustands ist definiert als:
S = kB ln w
Wo W Es ist die Anzahl möglicher mikroskopischer Zustände und kB Es ist Boltzmanns Konstante. Als ln w Es ist dimensionlos, die Entropie hat die gleichen Einheiten wie kB: Joule/k.
Dies ist die berühmte Gleichung in Boltzmanns Grabstein in Wien. Mehr als Entropie ist jedoch die Änderung der Relevanz:
Es kann Ihnen dienen: thermodynamische Variablen: Welche und Übungen wurden gelöstΔS = kB ln w2 - kB ln w1 = kB ln (w2/w1)
Wie wird K berechnetB?
Der Wert der Boltzmann -Konstante wird experimentell genau mit Messungen basierend auf Akustische Thermometrie, die unter Verwendung der Eigenschaft durchgeführt werden, die die Abhängigkeit von der Schallgeschwindigkeit in einem Gas mit der Temperatur derselben festlegt.
In der Tat wird die Schallgeschwindigkeit in einem Gas gegeben durch:

Badiabatisch = γP
Und ρ ist die Gasdichte. Für die vorherige Gleichung, P Es ist der Druck des fraglichen Gases und γ Es ist der adiabatische Koeffizient, dessen Wert für ein bestimmtes Gas in Tabellen gefunden wird.
Metrologieinstitute erleben auch andere Möglichkeiten, die Konstante zu messen, wie z Johnson Noise Thermometry, Das verwendet die thermischen Schwankungen, die zufällig in den Materialien auftreten, insbesondere in Treibern.
Gelöste Übungen
-Übung 1
Finden:
a) die kinetische Energie der durchschnittlichen Übersetzung UNDC Das hat ein ideales Gasmolekül bei 25 ° C
b) die kinetische Übersetzungsergie K der Moleküle in 1 Mol dieses Gases
c) die Durchschnittsgeschwindigkeit eines Sauerstoffmoleküls bei 25 ºC
Tatsache
MSauerstoff = 16 x 10 -3 kg/mol
Lösung
Zu) UNDC = (3/2) k t = 1.5 x 1.380649 x 10-23J. K-1 x 298 k = 6.2 x 10-einundzwanzig J
B) K = (3/2) n.R.T = 5 x 1 mol x 8.314 j/mol .K x 298 K = 3716 J
C) UNDC = ½ mv2, Unter Berücksichtigung, dass das Sauerstoffmolekül diatomisch und die Molmasse mit 2 multipliziert werden muss, wird es:
 -Übung 2
-Übung 2
Finden Sie die Änderung der Entropie, wenn 1 Mol Gas mit einem Volumen von 0 besetzt ist.5m3 Es dehnt sich aus, um 1 m zu besetzen3.
Lösung
ΔS = kB ln (w2/w1)
W2= 2NW1 (Es gab 24 Mikroskopische Zustände für den Start der 4 Münzen, denken Sie daran?)
Wobei n die Anzahl der in 0 vorhandenen Partikel ist.5 Mol Gas 0.5 x nZU:
ΔS = kB ln (2N W1/w1) = kB ln 2N= kB 0.5nZU ln 2 = 2.88 j/k
Verweise
- Atkins, p. 1999. Physikalische Chemie. Omega -Ausgaben. 13-47.
- Bauer, w. 2011. Physik für Ingenieurwesen und Wissenschaften. Band 1. Mc Graw Hill. 664-672.
- Giancoli, d. 2006. Physik: Prinzipien mit Anwendungen. 6. ... Ed Prentice Hall. 443 -444.
- Sears, Zemansky. 2016. Universitätsphysik mit moderner Physik. 14. Ed. Band 1. 647-673.
- Wenn neu definiert. Kelvin: Boltzmann Konstante. Erholt von: NIST.Regierung
- « Wie man sich bei einer geliebten Person in 9 Schritten entschuldigt
- Was ist Kameradschaft und wie man es 10 Schlüssel fördert? »

